Kuinka tehdä molekyylimalli muovailuvahasta?

Tylsällä tieteellisellä kielellä esitetty kemia tuskin kiinnostaa opiskelijaa. Mutta jos yhdistät visuaaliset apuvälineet, oppiminen on hauskempaa. On vielä mielenkiintoisempaa tehdä asettelu omin käsin. Tässä artikkelissa kerromme sinulle, kuinka voit tehdä mallin molekyylistä muovailuvahalla. Informatiiviseen oppituntiin minkä tahansa molekyylin rakenne sopii: rauta, alkoholi, hiilidioksidi. Tarkastellaanpa useita vaihtoehtoja yksityiskohtaisemmin. Muiden aineiden mallit tehdään samojen sääntöjen mukaan: muotoilemme atomeja muovailuvahasta ja rakenteellisiin sidoksiin käytämme hammastikkuja tai tulitikkuja.


Mikä on välttämätöntä?
Ennen kuin aloitat mallinnustunnin ja samalla kemian, sinun on valmisteltava seuraavat materiaalit:
- useiden sävyjen muovailuvaha;
- hammastikkuja tai tulitikkuja;
- lauta tai öljykangas plastiliinin kanssa työskentelyyn;
- Internetistä tai kemian oppikirjasta poimittuja molekyylikaavoja.
Kun kaikki on valmis, voit alkaa tehdä molekyylimallia mistä tahansa aineesta.


Kuinka muotoilla erilaisia malleja?
On parempi muotoilla välittömästi malli tietyn aineen molekyylistä kaavion mukaan kuin alkaa selittämään abstraktien tuotteiden mikroobjekteja. Ensin puhutaan elementtien rakenteellisista sidoksista eri aineiden esimerkillä: metaani, etaani, eteeni, metyleeni.
Selvyyden vuoksi muokkaamme jokaista valmistettua molekyyliä rakentamalla siitä kaavion seuraavasta kognitiivisesta mallista. Tämä ei ole vaikea tehdä, koska hiilen ja vedyn sidos on mukana kaikissa järjestelmissä.
Metaani
Otetaan ensin pohjaksi yksinkertainen maakaasumetaanimolekyyli, jonka kaava on CH4. Valmista vastaava malli pyörittämällä neljä pientä palloa sinisestä muovailuvahasta: ne edustavat vetyä. Valmista sitten punainen pallo, joka on useita kertoja suurempi kuin siniset, - hiili. Tee rakenteellisia sidoksia tulitikuilla lisäämällä vetyä hiileen 4. Tuloksena on yksinkertaisin metaanimolekyylin malli.


Ethane
Etaanin C2H6 orgaaninen yhdiste kaavamaisessa versiossa näyttää monimutkaisemmalta kuin metaani, mutta rakenteellisesti malli on tehty samoista plastiliiniosista ja tulitikuista, joten sen valmistaminen ei tule olemaan vaikeaa.
Poista metaaniveistoksesta yksi tulitikku, jossa on sininen elementti. Tämä jättää hiileen kaksi vetysidosta. Etaanin muodostamiseksi tarvitsemme kaksi tällaista joukkoa. Sidomalla ne yhteen ylimääräisellä tulitikulla saadaan etaaniyhdistettä.


Etyleeni
Eteenin mallintamiseksi teemme kaksoissidosrakenteen. Voit tehdä tämän poistamalla jokaisesta punaisesta pallosta yhden sinisillä elementeillä varustetun tulitikun etaanikuviosta ja lisäämällä toinen yhdystuli hiilipallojen väliin. Tässä on mitä meillä on.

Metyleeni
Nyt, käyttämällä metyleenin (CH2) esimerkkiä, opimme tekemään sidosketjun. Pyöritä tätä varten 3 samankokoista palloa: yksi punainen (hiili) ja 2 sinistä (vety).
Koostamme metyleenimolekyylin kaksoissidoksella kokoamalla ketjun seuraavan kaavion mukaisesti: vety-hiili-vety, eli yhdistämme sinisen pallon kahdella tulitikulla punaisella ja taas kahdella tulitikulla sinisellä pallolla. Liitämme kaikki elementit yhdelle riville.

Kognitiivisia tarkoituksia varten ehdotamme useiden erilaisten kemikaalien molekyylien keräämistä.
Propaani
Tämä kaasu kuuluu yhdisteisiin, jotka sisältävät 3 hiiliatomia ja 8 vetyatomia (C3P8). Tilamallia varten sinun on tehtävä muovailuvahasta 3 suurta punaista palloa ja 8 pientä sinistä hernettä. Tarvitsemme 10 tulitikkua yhdistäväksi siteeksi. Propaanimolekyylimallin kokoaminen suoritetaan seuraavalla tavalla.
- Kiinnitämme 3 sinistä hernettä yhteen punaisista palloista tulitikuilla.
- Monistamme rakenteen, koska tarvitsemme kaksi identtistä vaihtoehtoa.
- Lisää jäljellä olevaan kolmanteen punaiseen palloon kaksi tulitikuihin kiinnitettyä sinistä hernettä.
- Nyt yhdistämme kaikki kolme osaa yhteen. Keskellä pitäisi olla hiiliatomi, jossa on kaksi vetyatomia, ja reunoilla jokaisessa hiilessä tulisi olla 3 vetyatomia.
Propaanimolekyylin rakenteesta vastaava sidostyyppi on sama kuin butaanin, metaanin kaasuissa.


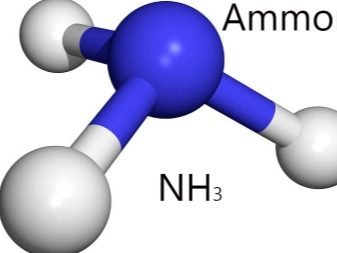
Ammoniakki
Se on typen ja vedyn (NH3) epäorgaaninen binäärinen yhdiste. Ammoniakki on väritön kaasu, joka on helposti tunnistettavissa ominaisesta hajusta. Aiemmissa malleissa käytimme sinistä muovailuvahaa vetyatomin muodostamiseen ja punaista hiiltä. Ammoniakkimolekyyliä mallinnettaessa käytä kolmelle vetyatomille myös sinistä, eli sokeaa 3 sinistä palloa.
Valitse typelle eri väri, kuten keltainen. Tarvitset yhden tämän sävyn pallon. Kiinnitä nyt tulitikkujen avulla 3 vetyä (sinistä palloa) typpeen (keltainen pallo). Ammoniakkimalli on valmis.

Kloori
Tämä halogeeni on laajalle levinnyt ympäröivässä maailmassa. Kaasun molekyylirakenne on erittäin yksinkertainen, se sisältää vain kaksi atomia (Cl2). Kloori on ilmaa raskaampaa, sillä on vihertävän keltainen sävy ja myrkyllinen, pistävä haju.
Sen molekyylien kuvaaminen ei ole vaikeaa. Sinun täytyy veistää kaksi vihreää palloa muovailuvahasta ja yhdistää ne yhdellä tulitikulla. Vielä helpompi tapa on kiinnittää kaksi palloa sivuttain toisiinsa ilman tulitikkuja tai hammastikkuja.

Suola
Monimutkainen aine, jota löytyy luonnosta eri muunnelmina, esimerkiksi natriumkloridi (NaCl), kalsiumsulfaatti (CaSo4). NaCl:a kutsutaan myös ruokasuolaksi, se on meille kaikille tuttu, koska se on elintarvikelaatuista.
Ruokasuolayhdisteen valmistamiseksi teemme kaksi palloa: pieni vihreä (kloori) ja suuri ruskea (natrium). Jotta niistä muodostuisi yksi molekyyli, riittää, että pallot puristetaan yhteen, mutta voit myös käyttää tulitikkua, joka symboloi yhdistäviä sidoksia.

Hyödyllisiä vinkkejä
Nykyaikaiset vanhemmat ja ilman neuvoja osaavat kehittää lapsiaan, mutta emme silti anna muutaman suosituksen.
Jos haluat välittää monimutkaista tietoa opiskelijalle, etsi epätyypillisiä tapoja esittää se. Meidän tapauksessamme kemiaa opetetaan 3D-mallinnuksella. Hyödylliset kohdat ovat seuraavat.
- Lapset oppivat uutta tietoa.
- Tiedonhankintamenetelmään liittyy luova tilavuuslukujen veistoprosessi. Se kiehtoo ja mahdollistaa opiskelijan kiinnostuksen niinkin monimutkaisesta aiheesta kuin kemia.
- Muovailuvahalla työskentely kehittää käsien motorisia taitoja, joten siitä on hyötyä henkiselle toiminnalle ja luovuudelle.
- Veistos auttaa kehittämään hyödyllisiä ominaisuuksia, kuten mielikuvitusta, sinnikkyyttä ja keskittymistä.
Aloita oppiminen yksinkertaisilla mutta todellisilla molekyylimalleilla. Lapsen tulisi välittömästi tuntea olevansa mukana todellisessa tieteessä.
Kutsu poikasi tai tyttäresi oppikirjan (Internet) avulla etsimään itsenäisesti molekyylien kaavat, joita et ole vielä läpäissyt. Anna lapsen tehdä malli ilman apua löydettyä suunnitelmaa ja mielikuvitusta käyttäen. Hän saattaa olla kiinnostunut siitä, mistä molekyyleistä ilma, happi, vesi, kulta, timantti tai makea sokeri koostuu.


Teemme muovailuvahasta edelleen mallin vesimolekyylistä.








